Unsur, Senyawa, Dan Campuran
Label:
Kimia,
Materi Pelajaran
Unsur, senyawa dan campuran (Plassa). Materi yang terdapat di bumi ini sangat beranekaragam dan tak terhitung jumlahnya. Mulai dari zat tunggal yang terdiri dari unsur
dan senyawa, sampai dengan campuran yang merupakan kumpulan berbagai
macam zat. Untuk memudahkan mempelajari materi tersebut dibuatlah
penggolongan materi sebagai berikut.
A. Penggolongan Materi
Air murni terdiri atas sejenis materi
yaitu air, sedangkan air laut terdiri dari air dan berbagai zat lain
yang terlarut atau tercampur di dalamnya, diantaranya adalah
garam-garam. Materi seperti air murni, tergolong ke dalam zat
tunggal/zat murni dan bersifat homogen. Zat tunggal artinya hanya
satu-satunya zat dan tidak ada zat lain selain dirinya serta bersifat
homogen artinya semua bagian zat itu bersifat serba sama baik sifat
fisis (wujud, warna, rasa, bau, dll.) dan sifat kimianya (rumus kimia, kereaktifan, dll.). Zat tunggal dibedakan atas unsur
dan senyawa. Sedangkan air laut terdiri dari berbagai jenis zat yang
disebut campuran dan bersifat heterogen yang meliputi koloid dan
suspensi.
Berikut adalah bagan penggolongan materi.
Berikut adalah bagan penggolongan materi.
Gambar 2.1 Bagan Penggolongan Materi
B. Unsur
1. Pengertian unsur
Unsur adalah zat tunggal yang tidak dapat diuraikan menjadi zat-zat lain yang lebih sederhana melalui reaksi kimia biasa. Bagian terkecil dari suatu unsur adalah atom. Beberapa contoh unsur adalah emas, perak, alumunium, tembaga, belerang, karbon, dan sebagainya. Sampai saat ini telah dikenal lebih dari 112 unsur, ada yang ditemukan dalam keadaan bebas, seperti emas dan intan, tetapi sebagian besar unsur ditemukan dalam keadaan terikat sebagai suatu senyawa. Unsur dapat dikelompokkan ke dalam unsur logam, nonlogam, dan metaloid/semilogam.
1. Pengertian unsur
Unsur adalah zat tunggal yang tidak dapat diuraikan menjadi zat-zat lain yang lebih sederhana melalui reaksi kimia biasa. Bagian terkecil dari suatu unsur adalah atom. Beberapa contoh unsur adalah emas, perak, alumunium, tembaga, belerang, karbon, dan sebagainya. Sampai saat ini telah dikenal lebih dari 112 unsur, ada yang ditemukan dalam keadaan bebas, seperti emas dan intan, tetapi sebagian besar unsur ditemukan dalam keadaan terikat sebagai suatu senyawa. Unsur dapat dikelompokkan ke dalam unsur logam, nonlogam, dan metaloid/semilogam.
Berikut adalah perbedaan antara unsur nonlogam dan logam yang diberikan pada tabel 2.1.
Tabel 2.1 Perbedaan Unsur Logam dan Nonlogam
Ada beberapa unsur yang memiliki sifat
seperti logam dan nonlogam. Unsur tersebut dikenal sebagai unsur
metaloid/ semilogam. Contohnya adalah silikon, boron, germanium, arsen
dan stibium (antimon). Unsur-unsur tersebut banyak digunakan sebagai
semikonduktor.
2. Tabel Periodik Unsur
Untuk memudahkan kita mempelajari unsur,
unsur tersebut ditampilkan dalam Tabel Periodik Unsur yang dikenal
sebagai Sistem Periodik Unsur (SPU). Dalam tabel periodik unsur-unsur
ada yang diletakkan pada lajur tegak (kolom) yang disebut golongan dan
lajur horizontal (baris) yang disebut periode. Pada satu golongan sifat unsur semakin mirip dan pada satu periode sifat unsur semakin berbeda.
Berikut adalah gambar Tabel Periodik Unsur.
Berikut adalah gambar Tabel Periodik Unsur.
Gambar 2.2 Tabel Periodik Unsur
3. Lambang Unsur
Untuk menyederhanakan nama unsur, para ilmuwan memberikan lambang unsur. Lambang unsur yang digunakan sampai sekarang dibuat oleh Jons Jacob Berzelius. Berikut adalah cara penulisan lambang unsur yang diusulkan oleh Jons Jacob Berzallius.
1. Setiap unsur dilambangkan dengan satu huruf dari huruf awal nama latinnya yang dituliskan dengan huruf kapital. Perhatikan contoh tabel berikut.
Tabel 2.5 Beberapa senyawa dan Unsur Penyusunnya
Tabel 2.6 Angka dalam Bahasa Yunani
Tabel 2.7 Beberapa senyawa dan Unsur Penyusunnya
Tabel 2.8 Beberapa senyawa dan Unsur Penyusunnya
Tabel 2.9 Beberapa senyawa dan Ion Penyusunnya
Tabel 2.10 Kation (Ion Positif)
Tabel 2.11 Anion (Ion Negatif)
2. Campuran heterogen
Campuran heterogen terdiri atas:
a. Suspensi
Ciri-ciri:
- Keruh
- Ada bidang batas antar komponen-komponen penyusunnya
- Dapat disaring
- Mengendap
- Terdapat lapisan (kompenen padat dan cair memisah)
Contoh:
- Campuran terigu dan air
- Campuran pasir dan air
- Bubuk kopi dan air
b. Koloid
Ciri-ciri:
- Keruh
- Ada bidang batas antar komponen-komponen penyusunnya (jika dilihat dengan mikroskop ultra)
- Dapat disaring dengan kertas saring ultra
- Komponen padat dan cair dapat memisah sendiri dalam waktu relatif lama
Untuk menyederhanakan nama unsur, para ilmuwan memberikan lambang unsur. Lambang unsur yang digunakan sampai sekarang dibuat oleh Jons Jacob Berzelius. Berikut adalah cara penulisan lambang unsur yang diusulkan oleh Jons Jacob Berzallius.
1. Setiap unsur dilambangkan dengan satu huruf dari huruf awal nama latinnya yang dituliskan dengan huruf kapital. Perhatikan contoh tabel berikut.
Tabel 2.2 Nama unsur dan Lambangnya
2. Jika Huruf awal dari nama latinnya
sama, maka diberi huruf lain yang dituliskan dengan huruf kecil.
Perhatikan contoh dalam tabel berikut.
Tabel 2.3 Nama Unsur dan Lambangnya
C. Senyawa
1. Pengertian Senyawa
Senyawa adalah zat tunggal yang secara kimia masih dapat diuraikan menjadi zat-zat lain yang lebih sederhana dimana sifatnya berbeda dengan zat semula. Bagian terkecil dari suatu senyawa adalah molekul (gabungan dua atom unsur/lebih lebih baik sejenis ataupun berbeda jenis. Contohnya gula pasir yang berwarna putih, berwujud padat, dan berasa manis jika dipanaskan sampai terbakar akan mengalami reaksi.
Berikut adalah hasil reaksinya.
Senyawa adalah zat tunggal yang secara kimia masih dapat diuraikan menjadi zat-zat lain yang lebih sederhana dimana sifatnya berbeda dengan zat semula. Bagian terkecil dari suatu senyawa adalah molekul (gabungan dua atom unsur/lebih lebih baik sejenis ataupun berbeda jenis. Contohnya gula pasir yang berwarna putih, berwujud padat, dan berasa manis jika dipanaskan sampai terbakar akan mengalami reaksi.
Berikut adalah hasil reaksinya.
- Sebelum reaksi: gula pasir berwujud padat, berwarna putih, dan berasa manis
- Setelah reaksi terdapat zat baru:
- Zat yang berwujud padat, berwarna hitam, dan berasa pahit (karbon)
- Titik-titik cairan, tak berwarna, tak berasa, tak berbau (air)
- Zat tak berwarna, tak berbau, dan mengeruhkan air kapur (karbon dioksida)
Berarti kita dapat mengetahui bahwa gula dapat dipecah menjadi karbon, air, dan gas karbon dioksida melalui reaksi pembakaran.
Air juga tergolong ke dalam senyawa. Air dapat diuraikan menjadi dua jenis zat lain, yaitu gas hidrogen dan oksigen. Penguraian air dapat terjadi jika uap air dipanaskan pada suhu tinggi atau jika air dialiri listrik. Sifat gas hidrogen dan oksigen berbeda dengan sifat air. Gas hidrogen mudah terbakar, sedangkan oksigen merupakan gas yang diperlukan pada proses pembakaran. Sementara air tidak dapat terbakar dan tidak dapat melangsungkan pembakaran.
- Titik-titik cairan, tak berwarna, tak berasa, tak berbau (air)
- Zat tak berwarna, tak berbau, dan mengeruhkan air kapur (karbon dioksida)
Berarti kita dapat mengetahui bahwa gula dapat dipecah menjadi karbon, air, dan gas karbon dioksida melalui reaksi pembakaran.
Air juga tergolong ke dalam senyawa. Air dapat diuraikan menjadi dua jenis zat lain, yaitu gas hidrogen dan oksigen. Penguraian air dapat terjadi jika uap air dipanaskan pada suhu tinggi atau jika air dialiri listrik. Sifat gas hidrogen dan oksigen berbeda dengan sifat air. Gas hidrogen mudah terbakar, sedangkan oksigen merupakan gas yang diperlukan pada proses pembakaran. Sementara air tidak dapat terbakar dan tidak dapat melangsungkan pembakaran.
Gambar 2.3 Penguraian Air menjadi Gas Hidrogen dan Oksigen oleh Arus Listrik
2. Lambang Senyawa/Rumus Kimia
Sama halnya dengan unsur, senyawa pun perlu diberi lambang. Lambang untuk senyawa disebut rumus kimia. Berikut adalah rumus kimia dari beberapa senyawa yang ditampilkan dalam tabel.
Sama halnya dengan unsur, senyawa pun perlu diberi lambang. Lambang untuk senyawa disebut rumus kimia. Berikut adalah rumus kimia dari beberapa senyawa yang ditampilkan dalam tabel.
Tabel 2.4 Nama Senyawa dan Rumus Kimianya
Secara umum rumus kimia dapat dituliskan:
n: Koefisien yang menunjukkan jumlah molekul
A, B, C: lambang atom unsur penyusun molekul senyawa
x. y, z: Indeks tiap atom unsur penyusun, yang menunjukkan banyaknya atom unsur dalam setiap molekul
Contoh:
2C6H12O6: 2 molekul glukosa disusun oleh 12 atom karbon, 24 atom hidrogen, dan 12 atom oksigen
3H2SO4: 3 molekul asam sulfat disusun oleh 3 atom sulfur, 6 atom hidrogen, dan 12 atom oksigen
A, B, C: lambang atom unsur penyusun molekul senyawa
x. y, z: Indeks tiap atom unsur penyusun, yang menunjukkan banyaknya atom unsur dalam setiap molekul
Contoh:
2C6H12O6: 2 molekul glukosa disusun oleh 12 atom karbon, 24 atom hidrogen, dan 12 atom oksigen
3H2SO4: 3 molekul asam sulfat disusun oleh 3 atom sulfur, 6 atom hidrogen, dan 12 atom oksigen
3. Tatanama Senyawa
Berdasarkan jenis unsur yang menyusun senyawa, senyawa dibedakan atas senyawa biner dan senyawa poliatom.
a. Senyawa Biner: Senyawa yang terdiri atas 2 jenis unsur
Senyawa biner dari logam dan nonlogam: nama logam disebut terlebih dahulu, kemudian nama nonlogam yang diberi akhiran –ida. Perhatikan contoh berikut.
Berdasarkan jenis unsur yang menyusun senyawa, senyawa dibedakan atas senyawa biner dan senyawa poliatom.
a. Senyawa Biner: Senyawa yang terdiri atas 2 jenis unsur
Senyawa biner dari logam dan nonlogam: nama logam disebut terlebih dahulu, kemudian nama nonlogam yang diberi akhiran –ida. Perhatikan contoh berikut.
Tabel 2.5 Beberapa senyawa dan Unsur Penyusunnya
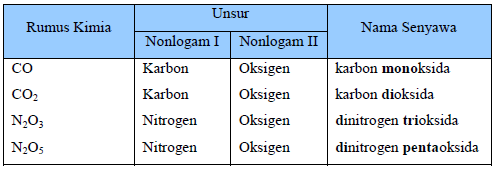
Senyawa biner dari nonlogam: nama
nonlogam yang ditulis pertama kali disebut terlebih dahulu, kemudian
nama nonlogam berikutnya yang diberi akhiran ida. Jika ada pasangan
unsur yang bersenyawa lebih dari satu jenis senyawa, maka penamaan
senyawa tersebut dapat dibedakan dengan menyebutkan angka indeksnya.
Angka-angka tersebut dinyatakan dalam bahasa yunani, yaitu sebagai
berikut.
Tabel 2.6 Angka dalam Bahasa Yunani
Perhatikan contoh berikut.
Tabel 2.7 Beberapa senyawa dan Unsur Penyusunnya
Senyawa biner dari hidrogen dan nonlogam
- Menggunakan kata hidrogen sebagai nama depan, dan nama nonlogam sebagai nama belakang, diberi akhiran ida.
- Menggunakan kata asam sebagai nama depan dan nama nonlogam sebagai nama belakang diberi akhiran ida.
- Menggunakan kata hidrogen sebagai nama depan, dan nama nonlogam sebagai nama belakang, diberi akhiran ida.
- Menggunakan kata asam sebagai nama depan dan nama nonlogam sebagai nama belakang diberi akhiran ida.
Tabel 2.8 Beberapa senyawa dan Unsur Penyusunnya
Senyawa poliatom: Senyawa ion (atom atau
gabungan atom yang bermuatan listrik) yang terdiri dari dua atau lebih
atom yang bergabung bersama-sama dalam satu ion. Penamaannya adalah nama
ion positif (kation) disebut terlebih dahulu kemudian nama ion negatif
(anion).
Tabel 2.9 Beberapa senyawa dan Ion Penyusunnya
Secara umum senyawa ion dapat dituliskan sebagai berikut.
Selengkapnya, perhatikan beberapa nama kation dan anion berikut
Tabel 2.10 Kation (Ion Positif)
Tabel 2.11 Anion (Ion Negatif)
D. Campuran
Seperti yang telah diuraikan di atas, air laut tergolong ke dalam campuran karena air laut terdiri atas air dan berbagai garam. Dari contoh tersebut kita dapat mengetahui bahwa campuran merupakan gabungan dua jenis zat atau lebih.
Campuran mempunyai sifat yang berbeda dengan senyawa. Dalam campuran sifat-sifat komponen tidak hilang. Ketika garam dapur dilarutkan dalam air, kedua zat itu tidak bersenyawa, melainkan bercampur.
Rasa garam sebelum dan sesudah dicampurkan tetap terasa asin, begitu pula dengan air. Air sebelum dicampurkan dan sesudah dicampurkan tetap dapat memadamkan api. Kemudian juga garam dengan air dapat bercampur dalam berbagai komposisi sesuai yang dikehendaki. Tidak demikian halnya dengan bersenyawa. Senyawa mempunyai kompisisi tertentu. Air sebagai contoh, terdiri dari hidrogen dan oksigen dengan perbandingan atom 2:1 Jadi, kita dapat menyatakan bahwa bersenyawa membentuk zat baru (berlangsung secara kimia), sedangkan bercampur tidak membentuk zat baru (berlangsung secara fisika).
Seperti yang telah diuraikan di atas, air laut tergolong ke dalam campuran karena air laut terdiri atas air dan berbagai garam. Dari contoh tersebut kita dapat mengetahui bahwa campuran merupakan gabungan dua jenis zat atau lebih.
Campuran mempunyai sifat yang berbeda dengan senyawa. Dalam campuran sifat-sifat komponen tidak hilang. Ketika garam dapur dilarutkan dalam air, kedua zat itu tidak bersenyawa, melainkan bercampur.
Rasa garam sebelum dan sesudah dicampurkan tetap terasa asin, begitu pula dengan air. Air sebelum dicampurkan dan sesudah dicampurkan tetap dapat memadamkan api. Kemudian juga garam dengan air dapat bercampur dalam berbagai komposisi sesuai yang dikehendaki. Tidak demikian halnya dengan bersenyawa. Senyawa mempunyai kompisisi tertentu. Air sebagai contoh, terdiri dari hidrogen dan oksigen dengan perbandingan atom 2:1 Jadi, kita dapat menyatakan bahwa bersenyawa membentuk zat baru (berlangsung secara kimia), sedangkan bercampur tidak membentuk zat baru (berlangsung secara fisika).
E. Jenis-Jenis Campuran
Campuran dapat berupa:
1. Campuran homogen
Ciri:ciri:
- Terdiri dari zat terlarut (solut) dan pelarut (solven). Biasanya, komponen yang lebih banyak jumlahnya disebut sebagai zat pelarut, sedangkan yang lebih sedikit disebut sebagai zat terlarut. Namun, jika larutan berwujud cair, maka komponen cair disebut sebagai zat pelarut.
- Serba sama, tidak ada bidang batas antar komponen-komponen penyusunnya
- Tidak dapat disaring
- Tidak terdapat lapisan (komponen padat dan cair tidak memisah)
Contoh:
- Udara - Air gula
- Sirup - Air cuka
- Air hujan - Spirtus
1. Campuran homogen
Ciri:ciri:
- Terdiri dari zat terlarut (solut) dan pelarut (solven). Biasanya, komponen yang lebih banyak jumlahnya disebut sebagai zat pelarut, sedangkan yang lebih sedikit disebut sebagai zat terlarut. Namun, jika larutan berwujud cair, maka komponen cair disebut sebagai zat pelarut.
- Serba sama, tidak ada bidang batas antar komponen-komponen penyusunnya
- Tidak dapat disaring
- Tidak terdapat lapisan (komponen padat dan cair tidak memisah)
Contoh:
- Udara - Air gula
- Sirup - Air cuka
- Air hujan - Spirtus
2. Campuran heterogen
Campuran heterogen terdiri atas:
a. Suspensi
Ciri-ciri:
- Keruh
- Ada bidang batas antar komponen-komponen penyusunnya
- Dapat disaring
- Mengendap
- Terdapat lapisan (kompenen padat dan cair memisah)
Contoh:
- Campuran terigu dan air
- Campuran pasir dan air
- Bubuk kopi dan air
b. Koloid
Ciri-ciri:
- Keruh
- Ada bidang batas antar komponen-komponen penyusunnya (jika dilihat dengan mikroskop ultra)
- Dapat disaring dengan kertas saring ultra
- Komponen padat dan cair dapat memisah sendiri dalam waktu relatif lama
- Dapat menghamburkan cahaya
Contoh:
- Air susu - Cat - Tinta
- santan - Asap - Kabut
c. Larutan
Contoh:
- Air susu - Cat - Tinta
- santan - Asap - Kabut
c. Larutan
Gambar 2.4 Campuran Homogen dan Heterogen







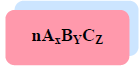










Tidak ada komentar:
Posting Komentar